Les cellules sont-elles chatouilleuses ?
Sciences et technologies
Article
Des micro-piliers en fer actionnables par un champ magnétique ont été incorporés dans une fine couche d’élastomère afin d’exercer sur des cellules des contraintes voisines de celles du milieu in vivo. Le dispositif enregistre à la fois la réponse mécanique et la réponse biochimique des cellules et permet d’en suivre l’évolution spatio-temporelle à une échelle sub-cellulaire.
L’environnement in vivo des cellules exercent sur elles des contraintes mécaniques qui varient, provoquant des réponses biochimiques intracellulaires : c’est ce qu’on appelle la mécanotransduction. Les cellules sont ainsi capables d’adapter en fonction de leur environnement des fonctions essentielles telles que la migration, la prolifération ou la différenciation. Un mauvais fonctionnement de la mécanotransduction est impliqué dans un ensemble varié de pathologies, cardiaques, osseuses ou cancéreuses par exemple.
Des travaux antérieurs in vitro destinés à mieux comprendre les mécanismes de la mécanotransduction ont déjà montré la sensibilité des cellules aux aspects spatiaux et temporels d’un stimulus mécanique. L’objectif ici est de se rapprocher des contraintes mécaniques de l’environnement cellulaire et d’étudier la coordination spatio-temporelle des signaux mécaniques et biochimiques de la cellule.
Une collaboration entre des physiciens de l’Institut Néel [1] et des biophysiciens du Laboratoire interdisciplinaire de physique [2] a permis de développer des substrats magnéto-actifs capables d’appliquer ce type de contraintes aux cellules qu’ils supportent et de mesurer simultanément la réponse mécanique des cellules et la réponse optique de marqueurs biochimiques. Pour réaliser ces substrats magnéto-actifs, des micro-piliers en silicium recouvert de fer doux magnétique (les dimensions sont de l’ordre de la dizaine de micromètres) sont insérés dans une couche d’élastomère formant ainsi un substrat continu dont la rigidité est voisine de celle du milieu cellulaire in vivo. Grâce à une paire d’électroaimants, le substrat peut être déformé localement, chaque pilier exerçant des forces de compression ou de traction de l’ordre de grandeur des forces cellulaires in vivo. À l’aide d’un microscope à épifluorescence, on mesure en temps réel la position de billes fluorescentes préalablement introduites dans le substrat. L’analyse des déplacements des billes fournit alors l’ensemble des contraintes mécaniques exercées par le pilier et par la cellule.
Les chercheurs ont montré que les cellules sont chatouilleuses : juste après une stimulation mécanique, les cellules sont agitées. Via la mécanotransduction, elles réagissent à la contrainte et se déforment localement, agissant en retour elles-mêmes sur leur environnement . La preuve de concept du suivi spatio-temporel sur une cellule vivante par l’enregistrement simultané via le microscope à la fois de la réponse mécanique (par la fluorescence des billes du substrat) et de la réponse biochimique (par la fluorescence de marqueurs intracellulaires) a été faite.
Ces substrats magnéto-actifs ouvrent ainsi la voie à des études plus quantitatives dans le but de comprendre la coordination spatio-temporelle des signaux mécaniques et biochimiques lors de la mécanotransduction.
Des travaux antérieurs in vitro destinés à mieux comprendre les mécanismes de la mécanotransduction ont déjà montré la sensibilité des cellules aux aspects spatiaux et temporels d’un stimulus mécanique. L’objectif ici est de se rapprocher des contraintes mécaniques de l’environnement cellulaire et d’étudier la coordination spatio-temporelle des signaux mécaniques et biochimiques de la cellule.
Une collaboration entre des physiciens de l’Institut Néel [1] et des biophysiciens du Laboratoire interdisciplinaire de physique [2] a permis de développer des substrats magnéto-actifs capables d’appliquer ce type de contraintes aux cellules qu’ils supportent et de mesurer simultanément la réponse mécanique des cellules et la réponse optique de marqueurs biochimiques. Pour réaliser ces substrats magnéto-actifs, des micro-piliers en silicium recouvert de fer doux magnétique (les dimensions sont de l’ordre de la dizaine de micromètres) sont insérés dans une couche d’élastomère formant ainsi un substrat continu dont la rigidité est voisine de celle du milieu cellulaire in vivo. Grâce à une paire d’électroaimants, le substrat peut être déformé localement, chaque pilier exerçant des forces de compression ou de traction de l’ordre de grandeur des forces cellulaires in vivo. À l’aide d’un microscope à épifluorescence, on mesure en temps réel la position de billes fluorescentes préalablement introduites dans le substrat. L’analyse des déplacements des billes fournit alors l’ensemble des contraintes mécaniques exercées par le pilier et par la cellule.
Les chercheurs ont montré que les cellules sont chatouilleuses : juste après une stimulation mécanique, les cellules sont agitées. Via la mécanotransduction, elles réagissent à la contrainte et se déforment localement, agissant en retour elles-mêmes sur leur environnement . La preuve de concept du suivi spatio-temporel sur une cellule vivante par l’enregistrement simultané via le microscope à la fois de la réponse mécanique (par la fluorescence des billes du substrat) et de la réponse biochimique (par la fluorescence de marqueurs intracellulaires) a été faite.
Ces substrats magnéto-actifs ouvrent ainsi la voie à des études plus quantitatives dans le but de comprendre la coordination spatio-temporelle des signaux mécaniques et biochimiques lors de la mécanotransduction.

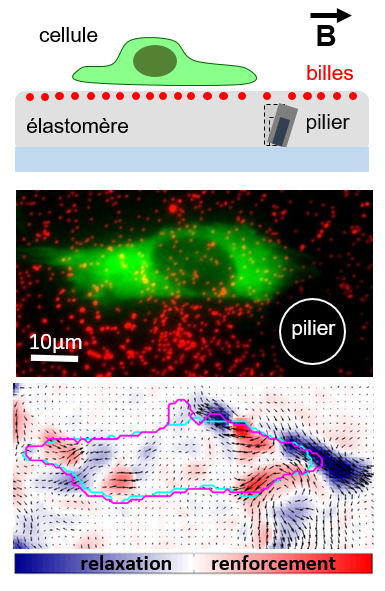
Haut : Schéma d’une cellule adhérente (en vert) sur le substrat élastomère contenant des micropiliers en fer et des billes fluorescentes (en rouge). B symbolise le champ magnétique permettant d’actionner le pilier.
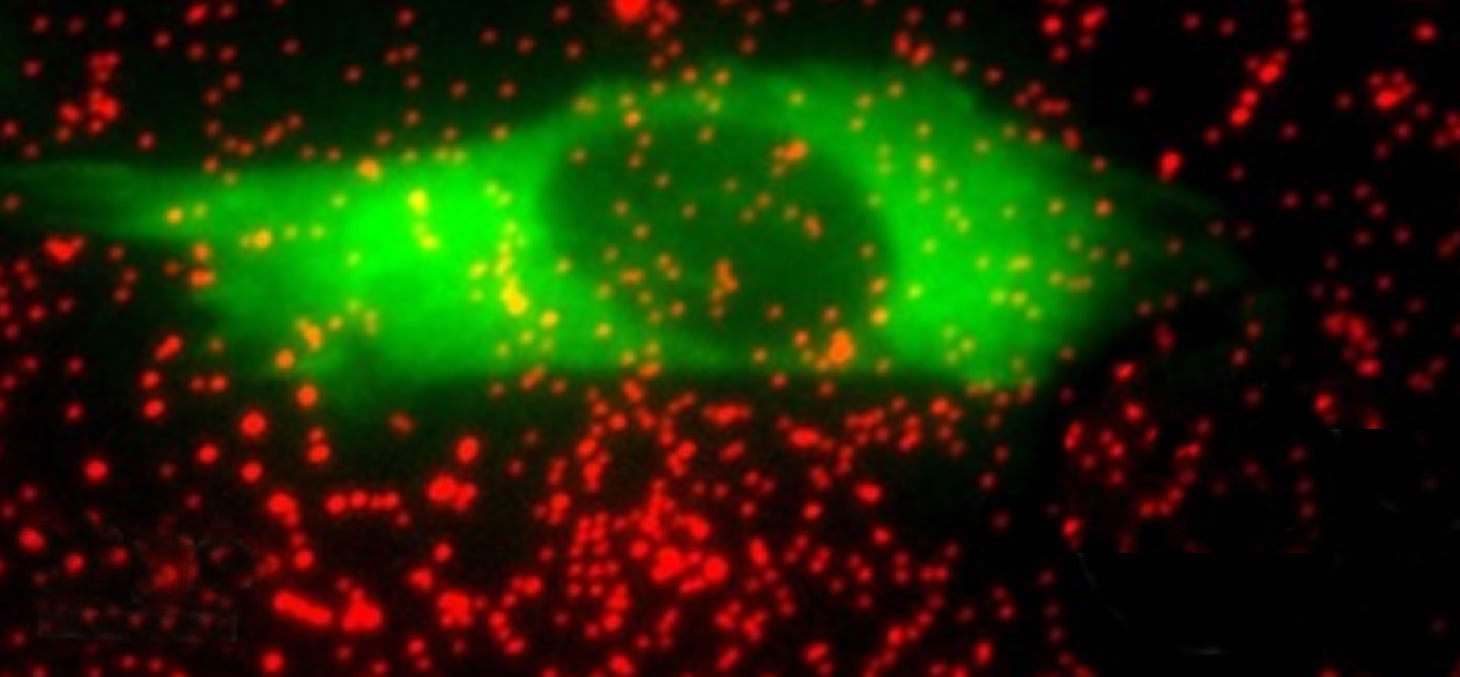
Milieu : Visualisation en microscopie de fluorescence de la cellule (marqueur fluorescent vert) et des billes (en rouge).
Bas : Carte des contraintes mécaniques montrant les zones que la cellule a renforcées (rouge) et celles qu’elle a relâchées (bleu) après la stimulation mécanique. Le contour de la cellule avant (cyan) et après (magenta) la stimulation de la cellule montre l’apparition une protubérance (en haut sur l’image).
© LIPhy (CNRS / Université Grenoble Alpes / Grenoble INP)
Milieu : Visualisation en microscopie de fluorescence de la cellule (marqueur fluorescent vert) et des billes (en rouge).
Bas : Carte des contraintes mécaniques montrant les zones que la cellule a renforcées (rouge) et celles qu’elle a relâchées (bleu) après la stimulation mécanique. Le contour de la cellule avant (cyan) et après (magenta) la stimulation de la cellule montre l’apparition une protubérance (en haut sur l’image).
© LIPhy (CNRS / Université Grenoble Alpes / Grenoble INP)
Publié le18 juin 2018
Mis à jour le19 juin 2018
Mis à jour le19 juin 2018
Vous aimerez peut-être aussi
- The Conversation Junior : "Alec et Eloa : « Pourquoi est-ce que quand on monte en haut d’une montagne il fait plus froid alors qu’on se rapproche du Soleil ? »"
- The Conversation : "Images de science : Le métal qui se prenait pour du verre"
- The Conversation : "Tuer pour la science ? Une nouvelle expérience de Milgram"
- The Conversation : "Le rêve de Jeff Bezos ou peut-on, vraiment, rajeunir en reprogrammant nos cellules ?"
Contact
Aurélie Dupont
Chargée de recherche CNRS
Chargée de recherche CNRS
Référence
Magneto-active substrates for local mechanical stimulation of living cells
Bidan C.M., Fratzl M., Coullomb A., Moreau P., Lombard A.H., Wang I., Balland M., Boudou T., Dempsey N., Devillers T. & Dupont A.
Scientific Reports (2018), doi:10.1038/s41598-018-19804-1
> Lire l’article sur la base d’archives ouvertes HAL
Bidan C.M., Fratzl M., Coullomb A., Moreau P., Lombard A.H., Wang I., Balland M., Boudou T., Dempsey N., Devillers T. & Dupont A.
Scientific Reports (2018), doi:10.1038/s41598-018-19804-1
> Lire l’article sur la base d’archives ouvertes HAL

