
Tout a commencé le 19 février 2020 par une communication du département de pharmacologie de l’université chinoise de Qingdao mentionnant l’activité antivirale du phosphate de chloroquine in vitro. Le trois mars, une équipe chinoise de la province de Guandong a publié un deuxième article faisant état des résultats du traitement d’une petite cohorte de 30 patients par une dose quotidienne de 400 mg d’hydroxychloroquine pendant 5 jours. Le critère d’évaluation principal était la négativation de la charge virale Covid-19 au niveau pharyngé après 7 jours. Cette étude ne mentionnait aucune différence significative entre le groupe traité et le groupe contrôle.
S’il n’existe pas pour l’instant de données faisant consensus concernant le Covid-19, l’histoire d’une potentielle activité inhibitrice de la chloroquine (et de son dérivé, l’hydroxychloroquine) contre les coronavirus n’est pas nouvelle. Elle remonte à l’épidémie de SARS-CoV, au début des années 2000. À l’époque, plusieurs équipes décrivent son activité antivirale par des investigations in vitro. Retour sur des molécules qui ont fait couler beaucoup d’encre.
La chloroquine est fabriquée par synthèse chimique. Il s’agit d’un dérivé de la quinine, un alcaloïde isolé en 1820 par deux pharmaciens-chimistes français, Pierre Joseph Pelletier et Joseph Bienaimé Caventou, à partir de l’écorce de quinquina, un arbuste originaire de l’Équateur et connu sous le nom d’« arbre à fièvre » par les Indiens des plateaux andins.
La chloroquine, initialement commercialisée sous le nom de Nivaquine, fut un médicament central de la lutte contre le paludisme. Elle fut très largement utilisée au cours des trois ou quatre décennies qui suivirent la Seconde Guerre mondiale, mais son intérêt dans cette indication est aujourd’hui devenu anecdotique. En effet, Plasmodium falciparum, l’espèce la plus répandue (et potentiellement mortelle) du parasite causant le paludisme a développé des résistances à la chloroquine à une échelle quasi mondiale.
Comme tout médicament, cette thérapeutique n’est cependant pas sans risque : une dose de 2 grammes de chloroquine est toxique, tandis que 4 grammes constituent une dose mortelle. La mise au point du sulfate d’hydroxychloroquine, mieux toléré par l’organisme, a constitué une alternative, qui reste toutefois soumise à prescription médicale en raison de sa marge thérapeutique étroite. Ce médicament n’est pas utilisé comme antipaludique, mais il est largement prescrit dans certaines maladies auto-immunes telles que la maladie lupique et la polyarthrite rhumatoïde, en raison de ses propriétés anti-inflammatoires. Les doses généralement prescrites sont de 600 mg/jour pendant plusieurs mois.
La chloroquine et l’hydroxychloroquine ont des effets thérapeutiques nombreux et complexes. Leur action majeure est liée à une inhibition des fonctions lysosomiales. Les lysosomes sont des vésicules présentes dans les cellules et contenant des enzymes. Actifs lorsque le pH est acide, ces derniers sont capables de digérer la plupart des composants de la cellule : protéines, sucres, lipides, acides nucléiques…
Il a été montré très tôt que la chloroquine a une remarquable affinité pour les lysosomes. Une fois concentrée à l’intérieur, elle en augmente le pH et perturbe ainsi leurs fonctions enzymatiques. Les scientifiques ont également découvert que la chloroquine et l’hydroxychloroquine stabilisent les membranes des endosomes, une autre sorte de vésicules présentes dans la cellule et impliquées dans le transit et le tri des molécules.
Cette propriété de la chloroquine explique son effet antipaludique. En effet, au cours de leur cycle de vie, les parasites responsables du paludisme pénètrent dans les globules rouges dont ils découpent l’hémoglobine pour fabriquer leurs propres protéines. Ils utilisent pour cela des enzymes contenus dans une vacuole digestive. En s’accumulant dans cette dernière, la chloroquine perturbe le fonctionnement enzymatique, à l’image de ce qui se passe dans les lysosomes.
Outre ces effets, la chloroquine influe à d’autres niveaux de l’organisme, en inhibant les fonctions des effecteurs de l’immunité innée (monocytes/macrophages) et spécifiques (activation lymphocytaire), ou en interférant avec certaines voies de signalisation cellulaires. Ces propriétés sont à l’origine de ses effets anti-inflammatoires, lesquels sont mis à contribution pour traiter les maladies auto-immunes telles que l’arthrite rhumatoïde.
Enfin, il a été prouvé que la chloroquine interfère avec la double hélice de l’ADN. Il s’agit donc d’un composé relativement toxique, présentant un risque de génotoxicité qui s’exprime principalement lors de son emploi en thérapie de longue durée.
Lors du traitement, les effets indésirables les plus courants sont des manifestations gastro-intestinales, comme les vomissements et la diarrhée. D’autres problèmes plus graves, tels qu’une atteinte de la rétine (rétinopathie) ou du cœur (cardiomyopathie) peuvent cependant survenir lors d’une exposition à long terme à la chloroquine. En outre, comme pour beaucoup de médicaments à marge thérapeutique étroite, il faut également impérativement surveiller la fonction rénale chez les sujets âgés, pour éviter les surdosages.
Chloroquine et hydroxychloroquine sont donc potentiellement capables d’interférer avec le développement des microorganismes qui infectent des cellules et détournent leurs lysosomes ou leurs endosomes à leur profit.
L’efficacité de la chloroquine a ainsi été prouvée dans le traitement de la fièvre Q, causée par la très infectieuse bactérie Coxiella burnetii, qui pénètre dans les cellules et peut provoquer des problèmes cardiaques graves, ou de la maladie de Whipple, due à une autre bactérie intracellulaire, qui nécessite un traitement à vie.
En ce qui concerne les virus, les choses sont moins claires. En 2005, des travaux menés sur des cellules de primates avaient mis en évidence une activité in vitro sur le virus SARS-CoV-1, responsable de l’épidémie de SARS de 2003. Le SARS-CoV-1 responsable de la maladie, ayant disparu, les chercheurs ont continué à tester l’activité de la chloroquine, notamment sur le MERS-CoV, avec des résultats encourageants in vitro.
En revanche, d’autres études avaient démontré une absence d’efficacité in vivo sur d’autres virus, tels que les virus du chikungunya, de la dengue, ou de la grippe.
Pour infecter une cellule, les virus commencent par s’accrocher à sa surface. Dans le cas des virus enveloppés, c’est-à-dire entourés par une membrane, tels que le SARS-CoV-2, l’étape suivante consiste à fusionner ladite membrane avec celle de la cellule. Selon les virus, cette fusion peut avoir lieu à la surface cellulaire ou dans des endosomes après internalisation de la particule virale.
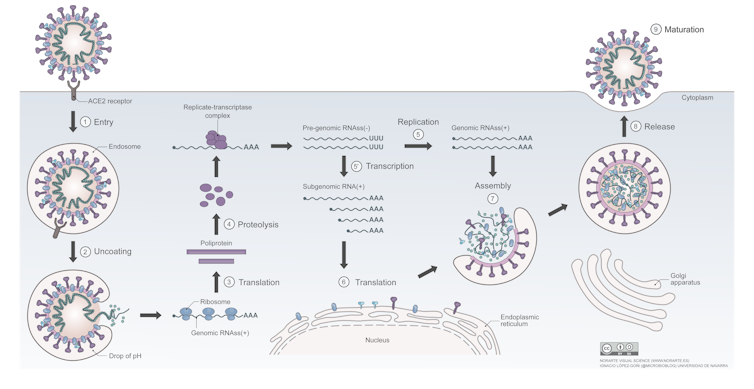
Dans le cas du coronavirus SARS-CoV-2, la chloroquine pourrait inhiber la fusion de la membrane virale avec la membrane cellulaire, prévenant ainsi le passage du virus dans le compartiment cytoplasmique. L’hydroxychloroquine inhibe également la réplication in vitro du SARS-CoV-2 dans les cultures cellulaires.
À ce stade des connaissances, il faut souligner que l’on considère que le passage des premiers symptômes de la maladie au syndrome de détresse respiratoire aiguë (SDRA) est très probablement dû à une libération incontrôlée de molécules favorisant l’infection, ce qui déclencherait un « orage inflammatoire ».
Tester la pertinence pharmacologique de la hydroxychloroquine n’est donc pas illogique : elle pourrait tenir à sa capacité à bloquer le coronavirus et à ses propriétés anti-inflammatoires. C’est dans cet esprit que, le 8 mars 2020, les chercheurs du Drug Clinical Trial Center à Pékin ont fait part de leur intérêt concernant le traitement des patients atteints de Covid-19 par l’hydroxychloroquine plutôt que la chloroquine.
Didier Raoult et son équipe, à l’IHU Méditerranée-infection à Marseille, ont dès lors décidé de conduire deux essais préliminaires. Les résultats du premier de ces essais, publiés le 20 mars 2020, indiqueraient qu’un traitement de huit jours, associant l’hydroxychloroquine avec un antibiotique de la série des macrolides, l’azithromycine, aboutirait à une « clairance virale » (le virus n’est plus détecté chez les patients ou dans des cultures cellulaires). Cet antibiotique est utilisé car il a été démontré que dans le cas de l’infection par le virus de la grippe A (H1N1), il interfère avec le processus d’internalisation du virus. D’autres études mentionnent une action antivirale sur des virus appartenant au genre Enterovirus.
Ces travaux ont fait l’objet de diverses critiques et discussions quant à leur méthodologie : petit nombre de patients, essai non randomisé, absence de groupe contrôle… En outre, une équipe de l’hôpital Saint-Louis n’est pas parvenue à reproduire les résultats concernant la clairance virale.
Il faudra donc d’autres essais cliniques sur des grandes cohortes pour savoir si les résultats observés in vitro se traduisent bien par des effets intéressants in vivo, et, si tel est le cas, pour évaluer les risques liés aux effets secondaires, déterminer la posologie optimale, les indications de ce médicament potentiel, etc.
Lancé le 22 mars, l’essai Discovery prévoit d’inclure 3 200 patient·es européen·nes. Alors que l’hydroxychloroquine en avait initialement été exclue, un bras de l’essai portera désormais sur son évaluation, mais sans l’associer à l’azithromycine. De son côté, le CHU d’Angers a lancé l’essai Hycovid, qui ambitionne de tester l’efficacité de cette molécule sur 1300 patients. Enfin, l’OMS envisage la tenue d’un essai contrôlé par placebo visant à évaluer la prophylaxie à la chloroquine sur le long terme. L’étude impliquerait 20 000 travailleurs de la santé, la chloroquine étant testée quotidiennement avec les doses utilisées pour la polyarthrite rhumatoïde.
Sauf énorme surprise, il faudra sans doute patienter encore plusieurs semaines avant de savoir avec certitude si les résultats des premières communications chinoises et françaises, qui portaient sur de petits effectifs de malades, seront confirmés (ou non) sur de plus grandes séries.![]()
Cet article est republié à partir de The Conversation sous licence Creative Commons. Lire l’article original.

